BMC Cancer volum 18 , Număr articol: 630 ( 2018 ) Citați acest articol
Abstract
fundal
Melanomul malign primar al vaginului este extrem de rar, cu un prognostic mai prost decât melanomul malign cutanat. Studiile anterioare au explorat reutilizarea itraconazolului, un agent antifungic oral comun, pentru tratamentul diferitelor tipuri de cancer. Aici, descriem o pacientă cu melanom malign vaginal metastatic, nerezecabil, tratată cu 200 mg itraconazol oral de două ori pe zi într-un studiu clinic cu o fereastră de oportunitate.
Prezentarea cazului
O japoneză în vârstă de 64 de ani cu tumori vaginale și inghinale a fost îndrumată la instituția noastră. Pe baza unui diagnostic inițial de cancer vaginal metastatic la ganglionii limfatici inghinali, am tratat-o cu itraconazol într-un studiu clinic până la obținerea rezultatelor studiului de biopsie și imagistică. În această perioadă, biopsiile au fost efectuate de trei ori și tomografia cu emisie de pozitroni 18 F-fluoro-deoxiglucoză (FDG/PET) – tomografie computerizată (CT) a fost efectuată de două ori. Rezultatele biopsiei au confirmat diagnosticul de melanom malign primar al vaginului. Studiile imagistice au dezvăluit metastaze în mai multe locuri, inclusiv în creier, pentru care ea a suferit o radiochirurgie gamma-knife. În perioada fereastră înainte de inițierea nivolumab, pacientul a primit itraconazol timp de 30 de zile. În decurs de o săptămână de la inițierea tratamentului cu itraconazol, durerea în ganglionii inghinali s-a ameliorat. PET-CT în zilele 6 și 30 a arătat o reducere a dimensiunii tumorii și, respectiv, a absorbției FDG. Specimenele biopsiate obținute în zilele 1, 13 și 30 au fost supuse analizei cu microarray ADNc, care a evidențiat o reglare descendentă de 100 de ori în transcrierea a patru gene: STATH , EEF1A2 , TTR și CDH2 . După 12 săptămâni de administrare de nivolumab, ea a dezvoltat boală progresivă și hepatită de gradul 3 asociată imunității. Întreruperea tratamentului cu nivolumab a dus la apariția durerii pelvine și inghinale stângi. După reprovocare cu itraconazol, pacientul nu a raportat nicio durere timp de 4 luni.
Concluzie
Descoperirile acestui caz sugerează că itraconazolul este o posibilă opțiune de tratament eficientă pentru melanomul malign primar al vaginului. Mai mult, am identificat potențiale gene țintă pentru itraconazol, care ar putea ajuta la elucidarea mecanismului care stă la baza acestei boli și ar putea ajuta la dezvoltarea de noi agenți terapeutici.
Rapoarte de evaluare inter pares
fundal
Melanomul malign primar al vaginului este extrem de rar și reprezintă aproximativ 5% din cancerele vaginale [ 1 ]. Prognosticul acestei afecțiuni este foarte prost în comparație cu prognosticul melanomului malign care apare din piele, din cauza stadiului clinic avansat la prezentare, iar un raport recent a arătat că vaginul fiind locul primar al melanomului este în sine un factor de prognostic independent [2] . ]. Tratamentul standard actual pentru melanomul nerezecabil sau recurent este inhibitorii punctelor de control imun, în timp ce inhibitorii RAF/MEK sunt utilizați și la pacienții simptomatici cu mutație BRAF [ 3 ]. Cu toate acestea, nu a fost stabilit un regim de tratament de linia a doua, iar dezvoltarea unor tratamente noi este justificată.
Itraconazolul, un agent antifungic oral comun, exercită activitate antitumorală prin modularea căilor de transducție a semnalului în celulele canceroase și fibroblastele asociate cancerului și prin inhibarea angiogenezei [ 4 ]. Mai multe studii clinice care au investigat reutilizarea itraconazolului ca agent anticancer împotriva diferitelor tipuri de cancer au dat rezultate promițătoare [ 5 , 6 , 7 , 8 , 9 , 10 , 11 ]. Liang şi colab. a sugerat că itraconazolul poate inhiba creșterea melanomului prin blocarea căilor țintei 3-kinaze-mamifere ale Hedgehog, Wnt și fosfatidilinozitol a rapamicinei (PI3K/mTOR) și a arătat că itraconazolul a prelungit supraviețuirea într-un model de melanom de șoarece xenogref in vivo [12 ] . Cu toate acestea, din cunoștințele noastre, efectul anticancer al itraconazolului asupra melanomului nu a fost investigat la om. Mai mult decât atât, melanomul vaginal este o afecțiune rară care este diferită genetic și molecular de melanomul cutanat [ 13 ] și nu se știe dacă itraconazolul este eficient împotriva melanomului vaginal.
În prezentul raport, descriem un caz de melanom malign vaginal metastatic, nerezecabil, tratat cu o cură de 30 de zile de itraconazol oral într-un studiu clinic cu o fereastră de oportunitate și a fost obținut un răspuns clinic precoce. Din câte cunoștințele noastre, acesta este primul raport al unui caz în care itraconazolul a fost utilizat pentru a trata melanomul malign primar al vaginului la un pacient uman și în care răspunsul și potențialele ținte au fost evaluate de 18 F-fluoro- deoxiglucoză . tomografie cu emisie de pozitroni (FDG/PET) – tomografie computerizată (CT) și, respectiv, microarray cADN tisular.
Prezentarea cazului
O femeie japoneză în vârstă de 64 de ani, multipară, a fost trimisă la instituția noastră cu antecedente de 1 an de sângerare vaginală anormală și antecedente de 2 luni de sângerare vaginală anormală și dureri inghinale stângi. Istoricul ei medical și familial nu era remarcabil și nu lua niciun medicament. Examenul ginecologic a evidențiat o leziune necrotică în relief, roșu-închis, cu diametrul de 5 cm, localizată pe peretele lateral stâng al vaginului proximal și o tumoră groasă nepigmentată în două treimi inferioare ale vaginului posterior. Colul uterin și fornixul păreau normale. Inghinala stângă era roșiatică și umflată, iar ganglionii limfatici inghinali măriți erau palpabili cu sensibilitate. Abdomenul ei inferior stâng era edematos. Am efectuat o biopsie a tumorii vaginale și am ajuns la un diagnostic preliminar de cancer vaginal nerezecabil cu metastaze la ganglionii limfatici inghinali.
Pacientul a fost informat despre un studiu clinic cu o fereastră de oportunitate înregistrat în Rețeaua de Informații Medicale a Spitalelor Universitare (UMIN 000018388), care a inclus terapia orală cu itraconazol și biopsii tumorale înainte și după tratamentul cu itraconazol. Consimțământul informat a fost obținut de la pacient pentru includerea în studiu. Astfel, în prima zi de trimitere, ea a fost începută cu 200 mg itraconazol pe cale orală de două ori pe zi și am planificat să continuăm acest regim de tratament până la obținerea rezultatelor biopsiei și efectuarea studiilor imagistice.
În ziua 1 de tratament cu itraconazol, dehidrogenaza ei lactică seric a fost ușor crescută (252 U/L) și antigenul de carcinom cu celule scuamoase a fost normal (1,1 ng/mL). Hemoleucograma și funcția hepatică au fost normale.
În ziua 6, constatările FDG/PET-CT au sugerat o tumoare vaginală și metastaze multiple la ganglionii limfatici inghinali, pelvini și para-aortici stângi și la piciorul drept (Fig. 1a – c ) . Cel mai mare diametru total al ganglionilor limfatici inghinali agregați a fost de 50 mm, iar valoarea maximă standard de absorbție (SUVmax) a fost de 19,8.
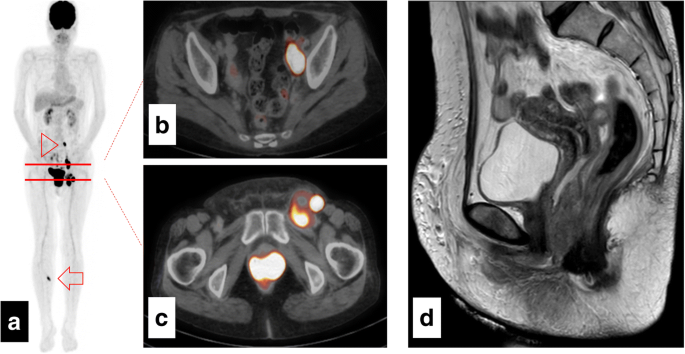
În ziua 7, ea a raportat ameliorarea durerii inghinale stângi. Examenul fizic a arătat că nodulii ei inghinali stângi s-au micșorat și că edemul s-a îmbunătățit.
În ziua 9, evaluarea microscopică a probei de biopsie a confirmat diagnosticul de melanom malign vaginal, cu colorare imunohistochimică pozitivă pentru HMB-45, S-100 și Melan A (Fig. 2 ) .
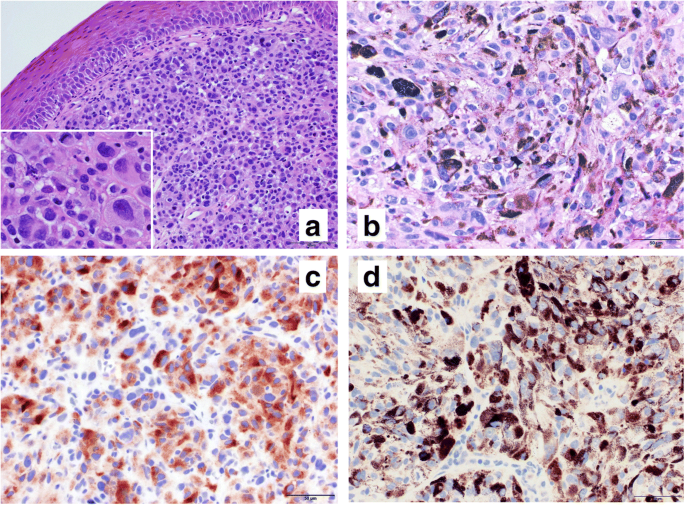
În ziua 13, imagistica prin rezonanță magnetică pelvină (IRM) a evidențiat un perete vaginal îngroșat (Fig. 1b ). Ulterior am efectuat o a doua biopsie vaginală în aceeași zi. RMN-ul capului efectuat în ziua 14 a evidențiat metastaze cerebrale. Fiecare dintre cele două tumori cerebrale a măsurat 1 cm în diametru, iar pacientul nu a prezentat dureri de cap sau simptome neurologice. În ziua 23, ea a suferit o radiochirurgie gamma-knife pentru metastaze cerebrale.
FDG/PET-CT efectuat în ziua 30 a arătat că diametrul ganglionilor limfatici inghinali agregați a scăzut la 38 mm, cu un SUVmax de 14,6 (Tabelul 1 ). Răspunsul general al tumorii a indicat o boală stabilă conform criteriilor de evaluare a răspunsului în tumorile solide (RECIST) versiunea 1.1 [ 14 ]. Testarea genetică a tumorii a dat rezultate negative pentru mutația BRAF , iar colorarea imunohistochimică a ligandului de moarte programată 1 (PD-L1) în ziua 30 a dat o rată de pozitivitate de 20%. Prin urmare, nivolumab a fost ales pentru tratamentul sistemic. Itraconazolul a fost întrerupt în ziua 30. O a treia biopsie vaginală a fost efectuată în ziua 30.Tabelul 1 18 Tomografie cu emisie de pozitroni F-fluor-deoxiglucoză – Constatări ale tomografiei computerizate
Specimenele biopsiate obținute în zilele 1, 13 și 30 au fost supuse analizei cu microarray ADNc. Acidul ribonucleic (ARN) a fost izolat din specimene și a fost supus analizei de microarray cADN utilizând kitul SurePrint G3 Human GE 8x60K v3 Microarray (Agilent Technologies, Tokyo, Japonia). Expresia modificată a genei a fost calculată ca log2 (nivelurile de ARN mesager [ARNm] în țesuturile tratate cu itraconazol față de nivelul de ARNm înainte de tratamentul cu itraconazol). Genele reglate în jos la < 1/32 din nivelurile de bază după 13 zile de administrare de itraconazol sunt enumerate în Tabelul 2 .Tabelul 2 Rezultatele analizei de microarray cADN tisular
În timpul tratamentului cu itraconazol, pacientul nu a prezentat reacții adverse și a rămas fără durere. Itraconazolul i-a atenuat și sângerarea genitală. În cele 5 zile dintre întreruperea tratamentului cu itraconazol și începerea tratamentului cu nivolumab, ganglionii ei inghinali stângi s-au mărit și abdomenul inferior stâng a devenit edematos, provocând dureri ușoare.
Inițierea tratamentului cu nivolumab (3 mg/kg, repetat la fiecare 2 săptămâni) ia îmbunătățit treptat simptomele; cu toate acestea, tumora vaginală primară a crescut în dimensiune după 10 săptămâni. După 12 săptămâni de administrare de nivolumab, pacientul a dezvoltat hepatită imună de grad 3 cu alanin transaminaze (ALT; 194 U/l) crescute, dar fără creștere a bilirubinei. Am întrerupt tratamentul cu nivolumab și am administrat imediat 1 mg/kg de metilprednisolon. După 6 zile, nivelul enzimelor ei hepatice a scăzut rapid la un nivel de gradul 1. Ea a dezvoltat dureri inghinale stângi și pelvine stângi, care au fost tratate cu supozitoare rectale de diclofenac. FDG/PET-CT a arătat creșterea tumorii vaginale primare și a crescut captarea 18-FDG atât în ganglionii limfatici metastatici, cât și în tumora vaginală primară. Pacientului i s-a administrat itraconazol, iar durerea ei s-a diminuat a doua zi. În timpul scăderii steroizilor de 6 săptămâni, ALT ei a crescut la 408 U/l și s-a readministrat 2 mg/kg de metilprednisolon. După 3 luni de reprovocare cu itraconazol, dimensiunea tumorii vaginale primare a crescut treptat. Cu toate acestea, o scanare CT a arătat că ganglionii limfatici metastatici au fost stabilizați și nu au fost găsite noi leziuni metastatice. RMN-ul capului a evidențiat remiterea metastazelor cerebrale. Nu a raportat nicio durere în cele 4 luni după reprovocarea cu itraconazol.
discutii si concluzii
Acest raport de caz oferă două perspective noi. În primul rând, din cunoștințele noastre, acesta este primul studiu care raportează un răspuns clinic obținut prin tratamentul cu itraconazol al melanomului malign primar și care evaluează răspunsul utilizând PET-CT. În al doilea rând, specimenele biopsiate au fost analizate prin microarray ADNc, oferind informații despre modificările expresiei genelor ca răspuns la tratamentul cu itraconazol.
Tratamentul cu itraconazol a dus la un răspuns clinic precoce. Ganglionii limfatici inghinali stângi ai pacientului au fost o țintă utilă pentru evaluarea vizuală și palpativă. În termen de o săptămână de la prima provocare cu itraconazol, ganglionii ei inghinali au fost mai mici la palpare și durerea i-a fost ameliorată. Ea a întrerupt tratamentul cu itraconazol după o perioadă de fereastră proiectată în studiul clinic și, ulterior, a experimentat durere inghinală stângă și edem cu creșterea tumorii. Progresia rapidă după încetarea itraconazolului pare a fi un fenomen de „aprindere”, care a fost raportat după întreruperea tratamentului cu inhibitori de tirozin kinaza [ 15 , 16 ]. Pentru a monitoriza răspunsul la itraconazol, am folosit FDG/PET-CT. Imagistica ganglionilor limfatici inghinali agregați a arătat o reducere cu 24% a dimensiunii tumorii și o reducere cu 26% a SUVmax. Deoarece itraconazolul s-a dovedit a fi eficient la acest pacient într-un studiu cu o fereastră de oportunitate, a fost utilizat pentru tratament, la un cost mai mic și cu efecte secundare minime, după întreruperea tratamentului cu nivolumab din cauza bolii progresive și a evenimentelor adverse legate de imun.
Melanomul malign este foarte vascular, iar expresia factorului de creștere a endoteliului vascular și a receptorilor săi sunt asociate cu un prognostic slab [ 17 , 18 ]. Un studiu prospectiv recent care a investigat reutilizarea propranololului ca agent anti-angiogeneză a arătat o supraviețuire îmbunătățită fără boală în rândul pacienților tratați cu propranolol cu melanom [ 19 ]. Itraconazolul are și activitate anti-angiogenetică. În 2007, Gupta et al. a verificat medicamentele aprobate de Administrația SUA pentru Alimente și Medicamente (FDA) și a identificat itraconazolul ca un agent anti-angiogenic promițător [ 20 ]. Prin urmare, itraconazolul ar putea inhiba creșterea celulelor melanomului prin inhibarea angiogenezei, precum și a fibroblastelor asociate melanomului [ 21 , 22 ].
Un studiu anterior a investigat efectul anti-melanom al itraconazolului in vitro și in vivo la șoareci [ 12 ], iar rezultatele au indicat că itraconazolul suprimă căile de semnalizare Hedgehog, Wnt și PI3K/mTOR în celulele melanomului. Aceste modificări de semnalizare au fost demonstrate și în celulele CaSki de cancer de col uterin tratate cu itraconazol [ 23 ]. În studiul de față, analiza microarray ADNc nu a evidențiat niciun efect al itraconazolului asupra căilor Hedgehog sau WNT/β-cateninei. Itraconazolul interferează cu căi multiple atât în celulele canceroase, cât și în celulele stromale din jur și au fost raportate anterior o varietate de efecte asupra diferitelor tipuri de celule canceroase [ 4 ]. Itraconazolul a inhibat angiogeneza prin inhibarea semnalizării AKT (protein kinaza B)/mTOR în celulele endoteliale ale venei ombilicale umane, care a fost rezultatul atât al metabolismului mitocondrial aberant, cât și al blocării traficului de colesterol [24 ] . Folosind linii celulare derivate din melanomul vaginal și alte afecțiuni maligne, am constatat că itraconazolul a inhibat transportul colesterolului în celulele canceroase (date nepublicate).
În cazul de față, analiza micromatricei ADNc tisular a dezvăluit rezultate interesante. Transcripțiile a patru gene ( STATH, EEF1A2, TTR și CDH2 ) au fost reglate în jos de 100 de ori. Gena STATH codifică statherina, EEF1A2 codifică factorul eucariotic de alungire a translației 1 alfa 2, TTR codifică transtiretina și CDH2 codifică N-caderina. Aceste rezultate diferă semnificativ de cele ale lui Liang et al. în celulele melanomului [ 12 ], iar reglarea în jos a acestor patru gene prin tratamentul cu itraconazol nu a fost raportată în rapoartele preclinice și clinice anterioare [ 4 ]. Acest lucru s-ar putea datora faptului că studiul nostru a fost efectuat pe un pacient uman și pentru că interacțiunile moleculare din melanomul vaginal ar putea fi diferite de cele din melanomul cutanat [ 13 ]. Am descoperit că itraconazolul a inhibat creșterea celulelor melanomului vaginal in vitro folosind o linie celulară, dar inhibarea căilor Hedgehog, Wnt sau PI3K/mTOR nu a fost observată (date nepublicate). Deși mecanismul precis care stă la baza activității anti-tumorale a itraconazolului la acest pacient este necunoscut, micromatricea ADNc tisular a dezvăluit modificări ale transcripției în celulele melanomului, precum și în micromediul înconjurător, oferind indicii despre mecanismele itraconazolului în țesutul uman.
S-a raportat că statherin joacă un rol în sănătatea orală, inclusiv în activitatea de protecție presupusă împotriva carcinogenezei [ 25 ]. Exprimarea ARN-ului sau proteinei statherinei nu a fost raportată în niciun alt organ la oamenii sănătoși [ 26 ] și, din câte cunoștințele noastre, nu au existat rapoarte de exprimare a statherinei în nicio altă afecțiune malignă, cu excepția cancerului oral. Plitidepsina, care vizează EFF1A2, a fost studiată în două studii clinice efectuate la pacienți cu melanom [ 27 , 28 ]. Duanmin și colab. au raportat că EEF1A2 este foarte exprimat în adenocarcinomul ductal pancreatic și este asociat cu metastaza ganglionilor limfatici [ 29 ]. Nu este clar din cazul de față dacă aceste constatări anterioare sunt aplicabile melanomului malign vaginal; sunt necesare studii suplimentare pentru a investiga acest lucru. Un studiu anterior privind utilizarea biomarkerilor serici pentru detectarea precoce a malignității a arătat că nivelurile de transtiretină au fost crescute în melanom, precum și în cancerul ovarian, endometrial și pulmonar; cu toate acestea, mecanismele care stau la baza prin care transtiretina este implicată în aceste cancere rămân necunoscute [ 30 , 31 , 32 , 33 ]. Tranziția de la E-cadherină la N-cadherină este o etapă esențială în migrarea și invazia celulelor canceroase, inclusiv a celulelor melanomului [ 34 ]. Transfecția in vitro a celulelor melanomului cu ARN interferent mic care vizează gena N-cadherină a dus la o scădere a activității metaloproteinazei-2 și -9 a matricei și a inhibat invazia [35 ] .
În concluzie, itraconazolul a fost eficient la un pacient cu melanom malign primar al vaginului. Răspunsul timpuriu la tratamentul cu itraconazol a fost evaluat cu FDG/PET-CT, iar metastazele ganglionare au fost bine controlate. Analiza microarray ADNc a țesutului biopsiat al tumorii vaginale a evidențiat o reglare în jos a genelor care ar putea fi ținta itraconazolului. Interacțiunea dintre itraconazol și aceste gene și efectele acestor interacțiuni justifică investigații suplimentare în studiile viitoare.
Abrevieri
AKT:
Protein kinaza BALT:
Alanin transaminazaCT:
Tomografie computerizataFDG/PET:
Tomografie cu emisie de pozitroni cu 18F-fluor-deoxiglucozăRMN:
Imagistică prin rezonanță magneticăARNm:
Acid ribonucleic mesagermTOR:
Ținta rapamicinei la mamiferePD-L1:
Ligand de moarte programat 1PI3K:
Fosfatidilinozitol 3-kinazaSUVmax:
Valoarea maximă de absorbție standard
Referințe
- Frumovitz M, Etchepareborda M, Sun CC, Soliman PT, Eifel PJ, Levenback CF, et al. Melanomul malign primar al vaginului. Obstet Gynecol. 2010;116(6):1358–65.Articol PubMed Google Academic
- Udager AM, Frisch NK, Hong LJ, Stasenko M, Johnston CM, Liu JR și colab. Melanoamele ginecologice: o analiză clinicopatologică și moleculară. Ginecol Oncol. 2017. https://doi.org/10.1016/j.ygyno.2017.08.023 .
- D’Angelo SP, Larkin J, Sosman JA, Lebbé C, Brady B, Neyns B și colab. Eficacitatea și siguranța Nivolumabului în monoterapie sau în asociere cu Ipilimumab la pacienții cu melanom al mucoasei: o analiză combinată. J Clin Oncol. 2017;35(2):226–35.Articol PubMed CAS Google Academic
- Tsubamoto H, Ueda T, Inoue K, Sakata K, Shibahara H, Sonoda T. Reutilizarea itraconazolului ca agent anticancer. Oncol Lett. 2017;14(2):1240–6.Articol PubMed PubMed Central Google Academic
- Rudin CM, Brahmer JR, Juergens RA, Hann CL, Ettinger DS, Sebree R și colab. Studiu de fază 2 al pemetrexedului și itraconazolului ca terapie de linia a doua pentru cancerul pulmonar non-squamos non-mici cu celule metastatice. J Thorac Oncol. 2013;8(5):619–23.Articol PubMed PubMed Central CAS Google Academic
- Antonarakis ES, Heath EI, Smith DC, Rathkopf D, Blackford AL, Danila DC și colab. Reutilizarea itraconazolului ca tratament pentru cancerul de prostată avansat: un studiu randomizat de fază II necomparativ la bărbați cu cancer de prostată metastatic rezistent la castrare. Oncolog. 2013;18(2):163–73.Articol PubMed PubMed Central CAS Google Academic
- Kim DJ, Kim J, Spaunhurst K, Montoya J, Khodosh R, Chandra K și colab. Studiu deschis, explorator de fază II, cu itraconazol oral pentru tratamentul carcinomului bazocelular. J Clin Oncol. 2014;32(8):745–51.Articol PubMed CAS Google Academic
- Tsubamoto H, Sonoda T, Yamasaki M, Inoue K. Impactul chimioterapiei combinate cu itraconazol asupra supraviețuirii pacienților cu cancer ovarian refractar. Anticancer Res. 2014;34(5):2481–7.PubMed CAS Google Academic
- Tsubamoto H, Sonoda T, Inoue K. Impactul itraconazolului asupra supraviețuirii pacienților pretratați intens cu cancer de sân triplu negativ. Anticancer Res. 2014;34(7):3839–44.PubMed CAS Google Academic
- Tsubamoto H, Sonoda T, Ikuta S, Tani S, Inoue K, Yamanaka N. Chimioterapie combinată cu itraconazol pentru tratarea cancerului pancreatic metastatic în a doua linie sau cadru suplimentar. Anticancer Res. 2015;35(7):4191–6.PubMed CAS Google Academic
- Tsubamoto H, Sonoda T, Ikuta S, Tani S, Inoue K, Yamanaka N. Impactul itraconazolului după chimioterapia de primă linie asupra supraviețuirii pacienților cu cancer de tract biliar metastatic. Anticancer Res. 2015;35(9):4923–7.PubMed CAS Google Academic
- Liang G, Liu M, Wang Q, Shen Y, Mei H, Li D și colab. Itraconazolul își exercită efectul anti-melanom prin suprimarea căilor de semnalizare hedgehog, Wnt și PI3K/mTOR. Oncotarget. 2017;8(17):28510–25.Articol PubMed PubMed Central Google Academic
- Hou JY, Baptiste C, Hombalegowda RB, Tergas AI, Feldman R, Jones NL, et al. Melanomul vulvar și vaginal: o subclasă unică de melanom mucoase bazată pe o analiză moleculară cuprinzătoare a 51 de cazuri, comparativ cu 2253 de cazuri de melanom nonginecologic. Cancer. 2017;123(8):1333–44.Articol PubMed CAS Google Academic
- Eisenhauer EA, Therasse P, Bogaerts J, Schwartz LH, Sargent D, Ford R și colab. Noi criterii de evaluare a răspunsului în tumorile solide: ghidul RECIST revizuit (versiunea 1.1). Eur J Cancer. 2009;45(2):228–47.Articol PubMed CAS Google Academic
- Desar IM, Mulder SF, Stillebroer AB, van Spronsen DJ, van der Graaf WT, Mulders PF și colab. Reversul victoriei: apariția simptomelor după întreruperea tratamentului cu sunitinib sau sorafenib la pacienții cu cancer de celule renale. Un raport de trei cazuri. Acta Oncol. 2009;48(6):927–31.Articol PubMed Google Academic
- Iacovelli R, Massari F, Albiges L, Loriot Y, Massard C, Fizazi K, et al. Dovezi și relevanță clinică a apariției tumorii la pacienții care întrerup tratamentul cu inhibitori de tirozin kinaza pentru tratamentul carcinomului renal metastatic. Eur Urol. 2015;68(1):154–60.Articol PubMed Google Academic
- Ugurel S, Rappl G, Tilgen W, Reinhold U. Creșterea concentrației serice a factorilor angiogenici la pacienții cu melanom malign se corelează cu progresia tumorii și supraviețuirea. J Clin Oncol. 2001;19(2):577–83.Articol PubMed CAS Google Academic
- Warso MA, Maniotis AJ, Chen X, Majumdar D, Patel MK, Shilkaitis A, et al. Semnificația prognostică a modelelor periodice acid-Schiff-pozitive în melanomul cutanat primar. Clin Cancer Res. 2001;7(3):473–7.PubMed CAS Google Academic
- De Giorgi V, Grazzini M, Benemei S, Marchionni N, Botteri E, Pennacchioli E, et al. Propranolol pentru tratamentul off-label al pacienților cu melanom: rezultate dintr-un studiu de cohortă. JAMA Oncol. 2017. https://doi.org/10.1001/jamaoncol.2017.2908.
- Gupta A, Unadkat JD, Mao Q. Interacțiunile agenților antifungici azolici cu proteina de rezistență la cancerul de sân uman (BCRP). J Pharm Sci. 2007;96(12):3226–35.Articol PubMed CAS Google Academic
- Zhou L, Yang K, Andl T, Wickett RR, Zhang Y. Perspective of targeting Cancer-associated fibroblasts in melanom. J Cancer. 2015;6(8):717–26.Articol PubMed PubMed Central CAS Google Academic
- Ziani L, Safta-Saadoun TB, Gourbeix J, Cavalcanti A, Robert C, Favre G, et al. Fibroblastele asociate melanomului scad susceptibilitatea celulelor tumorale la uciderea mediată de celulele NK prin secreția de matrice-metaloproteinaze. Oncotarget. 2017;8(12):19780–94.Articol PubMed PubMed Central Google Academic
- Ueda T, Tsubamoto H, Inoue K, Sakata K, Shibahara H, Sonoda T. Itraconazolul modulează ariciul, WNT/β-catenina, precum și Akt Signalling și inhibă proliferarea celulelor canceroase de col uterin. Anticancer Res. 2017;37(7):3521–6.PubMed Google Academic
- Head SA, Shi WQ, Yang EJ, Nacev BA, Hong SY, Pasunooti KK și colab. Dirijarea simultană a NPC1 și VDAC1 de către Itraconazol duce la inhibarea sinergică a semnalizării mTOR și a angiogenezei. ACS Chem Biol. 2017;12:174–82.Articol PubMed CAS Google Academic
- Contucci AM, Inzitari R, Agostino S, Vitali A, Fiorita A, Cabras T, et al. Nivelurile de statherin în saliva la pacienții cu leziuni precanceroase și canceroase ale cavității bucale: un raport preliminar. Dis. orală. 2005;11(2):95–9.Articol PubMed CAS Google Academic
- Atlasul proteinelor umane. https://www.proteinatlas.org/ENSG00000126549-STATH/tissue . Accesat la 6 mai 2018.
- Eisen T, Thomas J, Miller WH Jr, Gore M, Wolter P, Kavan P și colab. Studiu de fază II al plitidepsinei bisăptămânale ca terapie de linia a doua la pacienții cu melanom malign avansat. Melanom Res. 2009;19(3):185–92.Articol PubMed CAS Google Academic
- Plummer R, Lorigan P, Brown E, Zaucha R, Moiseyenko V, Demidov L și colab. Studiul de fază I-II al plitidepsinei și dacarbazinei ca terapie de primă linie pentru melanomul avansat. Br J Cancer. 2013;109(6):1451–9.Articol PubMed PubMed Central CAS Google Academic
- Duanmin H, Chao X, Qi Z. Expresia proteinei eEF1A2 se corelează cu metastaza ganglionilor limfatici și scăderea supraviețuirii în adenocarcinomul ductal pancreatic. Hepato-Gastroenterologie. 2013;60(124):870–5.PubMed CAS Google Academic
- Greco M, Mitri MD, Chiriacò F, Leo G, Brienza E, Maffia M. Profilul proteomic seric al melanomului malign cutanat și relația cu progresia cancerului: asociere cu activitatea alfa-N-acetilgalactosaminidazei derivate din tumoră. Rac Lett. 2009;283(2):222–9.Articol PubMed CAS Google Academic
- Kozak KR, Su F, Whitelegge JP, Faull K, Reddy S, Farias-Eisner R. Caracterizarea biomarkerilor serici pentru detectarea cancerului ovarian în stadiu incipient. Proteomica. 2005;5(17):4589–96.Articol PubMed CAS Google Academic
- Farias-Eisner G, Su F, Robbins T, Kotlerman J, Reddy S, Farias-Eisner R. Validarea biomarkerilor serici pentru detectarea cancerului endometrial în stadiu incipient și târziu. Am J Obstet Gynecol. 2010;202(1):73.e1–5.Articol CAS Google Academic
- Maciel CM, Junqueira M, Paschoal ME, Kawamura MT, Duarte RL, Carvalho Mda G, et al. Modelul proteomic diferențial seric al proteinelor cu greutate moleculară mică exprimat de pacienții cu cancer pulmonar cu adenocarcinom. J Exp Ther Oncol. 2005;5(1):31–8.PubMed Google Academic
- Lade-Keller J, Riber-Hansen R, Guldberg P, Schmidt H, Hamilton-Dutoit SJ, Steiniche T. Comutarea E-la N-cadherină în melanom este asociată cu scăderea expresiei fosfatazei și a omologului tensinei și cu progresia cancerului. Br J Dermatol. 2013;169(3):618–28.Articol PubMed CAS Google Academic
- Ciołczyk-Wierzbicka D, Laidler P. Inhibarea invaziei celulelor melanomului uman prin distrugerea N-cadherinei. Med Oncol. 2018;35(4):42.Articol PubMed PubMed Central CAS Google Academic
Finanțarea
Această lucrare a fost susținută de o subvenție KAKENHI a Societății Japoneze pentru Promovarea Științei (nr. JP17K11306 către Inoue K.), care a oferit sprijin financiar pentru investigarea efectelor antitumorale ale itraconazolului și a fost utilizată pentru achiziționarea de micromatrice și anticorpi.
Disponibilitatea datelor și materialelor
Toate datele prezentate în manuscris sunt disponibile de la autorul corespunzător, la cerere rezonabilă.
Informatia autorului
Autori și afilieri
- Departamentul de Obstetrică și Ginecologie, Colegiul de Medicină Hyogo, 1-1 Mukogawa, Nishinomiya, Hyogo, 663-8501, JaponiaKayo Inoue, Hiroshi Tsubamoto, Roze Isono-Nakata și Kazuko Sakata
- Departamentul de Oncologie Medicală, Spitalul Meiwa, Nishinomiya, Hyogo, 663-8186, JaponiaHiroshi Tsubamoto
- Departamentul de Patologie Chirurgicală, Colegiul de Medicină Hyogo, 1-1 Mukogawa, Nishinomiya, Hyogo, 663-8501, JaponiaNami Nakagomi
Contribuții
KI, HT și KS au scris manuscrisul și au participat la analiza și interpretarea datelor. RIN a participat la colectarea și interpretarea datelor de caz. NN a participat la interpretarea datelor. Toți autorii au participat la redactarea și revizuirea lucrării și au aprobat manuscrisul final.
autorul corespunzator
Declarații de etică
Aprobarea etică și acordul de participare
Acest studiu a făcut parte dintr-un studiu clinic intitulat „Evaluarea prospectivă a efectelor moleculare ale itraconazolului ca agent anti-cancer: un studiu de oportunitate”, care a fost aprobat de consiliul de evaluare instituțional al Colegiului de Medicină din Hyogo (nr. 282). ). Autorii au obținut consimțământul informat scris și consimțământul pentru publicare de la pacient.
Consimțământ pentru publicare
A fost obținut consimțământul informat scris de la pacient pentru publicarea acestui raport de caz și imaginile însoțitoare. O copie a consimțământului scris este disponibilă pentru revizuire de către editorul acestei reviste.
Interese concurente
Autorii declară că nu au interese concurente.
Nota editorului
Springer Nature rămâne neutră în ceea ce privește revendicările jurisdicționale din hărțile publicate și afilierile instituționale.
Drepturi și permisiuni
Acces deschis Acest articol este distribuit în conformitate cu termenii licenței internaționale Creative Commons Attribution 4.0 ( http://creativecommons.org/licenses/by/4.0/ ), care permite utilizarea, distribuirea și reproducerea fără restricții în orice mediu, cu condiția să oferiți merită adecvată autorului(i) original(i) și sursei, furnizați un link către licența Creative Commons și indicați dacă s-au făcut modificări. Renunțarea la Creative Commons Public Domain Dedication ( http://creativecommons.org/publicdomain/zero/1.0/ ) se aplică datelor puse la dispoziție în acest articol, cu excepția cazului în care se specifică altfel.